Харчова сода: формула хімічна. Хімічна формула питної соди і її застосування
Мабуть, на кожній домашній кухні є сода -непоказна коробочка з порошкоподібною речовиною. Господині використовують її як кулінарну добавку для приготування випічки. Однак сфера її застосування настільки широка, що речовина можна з упевненістю назвати універсальним помічником людини. Але що ж являє собою сода? У яких видах вона існує і як використовується в повсякденному житті?

назви соди
Перш ніж перейти до хімічними властивостями соди,варто згадати про те, що свою назву - «сода», речовина отримала від назви рослини солянка содоносная, зола якого була джерелом видобутку соди.
У хімії, сода - це узагальнююча назва солей натрію вугільної кислоти:
- Na2CO3 (Натрію карбонат) - хімічна формула кальцинованої соди;
- Na2CO3· 10H2O - господарська сода;
- NaHCO3 - харчова сода. Це і хімічна формула питної соди;
- Na2CO3· H2O або Na2CO3· 7H2O - хімічна формула кристалічної соди.
У повсякденному житті, а також у хімічній промисловості існують кілька тривіальних найменувань речовини:
- харчова сода;
- питна сода;
- натріюбікарбонат;
- добавка Е500;
- декагідрат натрію.

емпірична формула
Хімічна формула харчової соди - NaHCO3. Це кисла сіль вугільної кислоти. Якщо скласти атомні ваги всіх складових її елементів, то виходить атомна маса соди, рівна 84 а. е.
Спосіб її освіти вельми простий. Хімічна формула соди харчової - це комплексна взаємодія гідроксиду натрію з вугільною кислотою:
NaOH + H2CO3 = NaHCO3 + H2O.
В області хімії натрій двууглікіслий являє собоюкомплекс катіона натрію і аніону гідрокарбонату. При впровадженні цих елементів в організм, вони нормалізують кислотно-лужний баланс, нейтралізуючи надлишки кислот, що містяться в рідкому середовищі.
кальцинована сода
Хімічна формула кальцинованої соди - Na2CO3. Кальцинована сода - це біле, сипуча речовина, яке може бути представлено у вигляді гранул (А) або порошку (Б).
Такий вид соди має ряд особливостей, що відрізняють кальциновану соду від харчової.
- pH середовища. І харчова, і кальцинована сода - це луг, але перша - слабка, з pH = 8, а друга - сильна, з pH = 11. Про характер середовища свідчить і хімічна формула технічної соди.
- Галузь застосування. Харчова сода використовується в харчовій сфері, косметології та медицині. Кальцинована застосовується в якості дієвого засобу для чищення.
У домашньому господарстві за допомогою кальцинованої соди можна:
- займатися пранням, використовуючи її як пральний порошок;
- мити підлогу, однак для ламінату та паркету це засіб не підійде, оскільки воно може зіпсувати покриття;
- усувати трубні засмічення;
- чистити вироби з фаянсу.
При використанні кальцинованої соди потрібно бути гранично обережним, оскільки речовина дуже токсична, що відноситься до третьої групи небезпечних засобів.

Фізичні властивості харчової соди
Бікарбонат натрію являє собою порошкоподібну речовину білого кольору. Це комплекс елементів натрію, водню, вуглецю і кисню.
За щільністю порошок дорівнює 2,16 г / см3.

При температурних показниках +50про-60проЗ речовина починає плавитися.
Гідрокарбонат натрію, або питна сода представлена у вигляді порошку молочного кольору. У водному середовищі добре розчинний. Не горить. Хімічна формула питної соди така ж, як і у харчовій.
розчин соди

Харчова сода - речовина, яка повністю розчиняється у воді, в результаті чого виходить содовий розчин. Він застосовується в гігієнічних цілях як засіб полоскання ротової порожнини.
Хімічна формула розчину соди виглядає наступним чином:
NaHCO3 + H2O = H2CO3 + NaOH.
Водний розчин соди наділений слаболужним характером.
Натрій двууглікіслий у водному розчині дисоціює з утворенням наступних іонів:
Na2CO3 ↔ 2Na+ + CO32-
Властивості соди як лугу
Як вже неодноразово згадувалося, гідрокарбонатнатрію являє собою лужний речовина. Цей факт позначається на застосуванні соди як засобу для нейтралізації підвищеної кислотності організму, зокрема шлунка. Елементи, що утворюють речовину, мають безпечним впливом.
Сода підвищує працездатність нирок, оскількививодиться сеча має лужний середовищем. Крім того, вона зберігає необхідну кількість глутамінової АК в організмі, яка перешкоджає появі кам'яних утворень в нирках.
Лужне середовище допомагає кращому засвоєнню деяких вітамінів групи В: В1, В4, В5, В6 і В12.
При вживанні соди для доброго засвоєння їїпоєднують з гарячим молоком. Це сприяє тому, що у відділах тонкого кишечника сода взаємодіє з амінокислотами молока, в результаті чого з'являються натрієві солі амінокислот, що володіють лужним характером. Ці амінокислоти набагато краще, ніж сода, проникають в кров'яне русло, підвищуючи тим самим лужні запаси організму.
Каустична сода
Хімічна формула каустичної соди - NaOH. Структурна формула: Na - O - H.
Молекулярну масу речовини становлять атомні ваги, що утворюють його компонентів Na, O і H. Вона дорівнює 40.
Каустик добре розчинний у воді.
У промисловості по відношенню до цього виду соди застосовуються такі назви:
- їдкий натр;
- гідроксид натрію;
- гідрат окису натрію.
При роботі з каустичною содою необхідно використовувати захисні елементи одягу, оскільки при зіткненні зі шкірою вона залишає сильні опіки.
Сода в комплексі з оцтом
Хімічна формула оцту і соди є реакцією гасіння, при якій утворюються вода, вуглекислий газ і сіль оцтової кислоти.
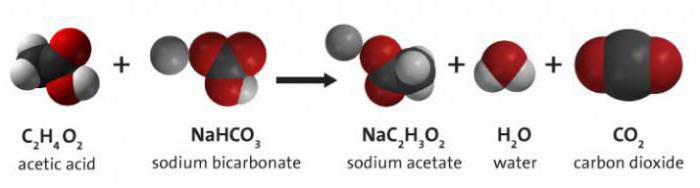
Даний хімічний "досвід" відбувається в супроводі характерного шипіння, яке свідчить про початок "спалюванні" соди.
Таку реакцію проводять в кулінарній справі, колимають намір замісити тісто для випічки. Оцет для цього беруть в концентрації 9%. Аналогом кислоти може виступати лимонний сік, яблучний або винний оцет.
Так навіщо ж проводити цю реакцію в приготуванні тесту? Справа вся в тому, що вийшов при розкладанні соди вуглекислий газ надає тісту пишності.
отримання речовини
Колись соду добували з золи рослини солянкисодоносной. В даний час основою для отримання цієї речовини є натуральний натрію сульфат. Реакція отримання виглядає наступним чином, де в правій частині відображена хімічна формула соди:
Na2SO4 + 3C + 2O2 = 2Na2CO3 + CO2 + 2SO2;
CaCO3 + C + Na2SO4 = Na2CO3 + 4CO + CaS.
Застосування харчової соди
Сода вельми популярна в повсякденному житті, причому не тільки як кулінарний компонент. Але розглянемо докладніше випадки, де використовується сода.
- Для початку варто зайвий раз згадати, що сода -харчової компонент в кулінарній справі. Її застосування не випадково: при нагріванні речовина здатна виділяти пари вуглекислого газу, що, в свою чергу, надає тісту легкості. В цьому випадку сода діє як розпушувач. Але якщо придбати в магазині пакетик з кондитерським розпушувачем тесту, то на упаковці в рядку складу можна виявити присутність соди, яка позначається як харчова добавка Е500.
- Використовують харчову соду і для виробництва газованих напоїв.
- Дуже часто соду використовують в так званій«Народної» медицині. У цій області сода виступає панацеєю практично при будь-яких недугах, наприклад, її ефективність доведена при печії, кашлі, при болях в горлі, шлунку, при підвищеній температурі.
- Непогано проявила себе харчова сода і як засіб длязасіб. Використовувати її можна для чищення сантехніки, алюмінієвих каструль, посуду, килимів, срібла і для прання білизни. Речовина має гарний знезаражувальним і протигрибковим засобом.
- Багато жінок використовують соду і в косметичнихі в гігієнічних цілях. Її можна використовувати як скраб для шкіри. Засіб відмінно позбавить від грубої шкіри стоп, якщо використовувати її для ножних ванн. З її допомогою можна позбутися від запаху поту як в області пахв, так і у взутті.
Допоможе сода і в відбілюванні зубів. Це недорогий, але ефективний спосіб. Порошок соди змішують із зубною пастою або водою і м'якими рухами проводять чистку зубів.
Каустична сода: застосування
Використання цього виду соди повинно бути в супроводі певних заходів безпеки, оскільки каустична сода - сильний луг, здатна «роз'їдати» багато типів поверхонь.
Для чого ж може бути корисно каустичної засіб в побутових умовах?
- Каустик прекрасно справляється з різнимизабрудненнями на посуді. Але варто утриматися від застосування цього засобу для виробів з алюмінію і тефлону. А ось для інших каструль, сковорідок або листів - будь ласка. Нагар, накип, застарілі шари жиру - з усім цим легко впорається каустик.
- Каустичною содою можна вирішити проблему засмічені труб. Необхідно просто засипати гранульована речовина в трубу і залишити на деякий час, після чого промити проточною водою.
Їдкий натр, він же каустична сода, широко застосуємо на промисловому рівні в різних областях виробництва.
- В будівництві. Тут речовина використовується для виготовлення деяких видів будівельних матеріалів, а також служить додатковим компонентом, що зміцнює фундаментальну основу споруд.
- У харчовій промисловості. Каустична сода може бути застосована і при виготовленні харчових продуктів. Зрозуміло, в цьому випадку вона використовується в слабкої концентрації. З її участю виробляють какао-порошки та шоколад, морозиво, карамелі, у випічці хліба, її застосовують як добавки Е524.
- Текстильна промисловість. У цій сфері каустична сода може бути застосована при відбілюванні тканин і для регенерації гумових виробів.
- Хімічне виробництво: каустична сода використовується як нейтралізатор кислот, засіб для очищення нафти і продуктів на її основі. Виробництво технічних масел також не обходиться без додавання каустичної соди. Крім того, їдкий натр - хороший каталізатор деяких хімічних реакцій.
- Чи можна застосувати каустична сода і для миловаріння при виробництві різних видів мила, шампунів і гелів.
Кальцинована сода: використання
Кальциновану соду також називають білизняний. Особливою затребуваністю це засіб користувалося ще в Радянському Союзі, отже, можна стверджувати: Білизна сода перевірена часом.
Застосовується засіб у наступних ситуаціях:
- Під час прання речей.
- При чищенні поверхонь кахлю, кераміки, фаянсу.
- При видаленні засмічення в трубах.
- Для ліквідації накипу в барабанах пральних машин, а також на посуді.
- Для знищення шкідливих комах на городах.
З вищесказаного висновок напрошується сам собою: сода універсальний засіб, що використовується в більшості сфер як побутової, так і промислової життя.
Позитивною якістю речовини є і те, що придбати її можна за сущі копійки.
</ P>


